Volumen 22 - Número 2 - Abril-Junio 2014
Protocolo en pérdida visual en paciente neoplásico
A. Filloy, S. Muñoz, J. Arruga
Hospital Universitari de Bellvitge. L’Hospitalet de Llobregat. Barcelona
CORRESPONDENCIA
Silvia Muñoz
Hospital Universitari de Bellvitge
Feixa Llarga s/n
08907 L’Hospitalet de Llobregat
E-mail: smq@bellvitgehospital.cat
Hospital Universitari de Bellvitge
Feixa Llarga s/n
08907 L’Hospitalet de Llobregat
E-mail: smq@bellvitgehospital.cat
RESUMEN
La pérdida visual en pacientes con antecedentes de enfermedad maligna puede estar producida por causas exclusivas que no van a aparecer en otro grupo de pacientes. Bien secundaria a los efectos indeseables de los tratamientos que ha recibido (yatrogénica), bien por efectos a distancia (paraneoplásica), o por progresión o diseminación de la enfermedad, es de extremada importancia realizar un correcto diagnóstico ya que puede representar un cambio radical en su pronóstico vital. Se describen los mecanismos de afectación visual y se proporciona un algoritmo para el manejo clínico de estas situaciones.
RESUM
La pèrdua visual en pacients amb antecedents de malaltia maligna pot estar produïda per causes exclusives que no apareixen en un altre grup de pacients. Bé secundària als efectes indesitjables dels tractaments rebuts (iatrogènica), bé sigui per efecte a distància (paraneoplàsica), o per progressió o disseminació de la malaltia, és de gran importància realitzar un correcte diagnòstic ja que pot representar un canvi radical en el pronòstic vital. Es descriuen els mecanismes d’afectació visual i es proporciona un algoritme per l’arranjament clínic en aquestes situacions.
ABSTRACT
Visual loss in patients with previous malignant disease may be produced by exclusive causes that would not be expected in non-neoplastic patients. Whether secondary to treatments applied, to cancer remote effects, or to malignancy progression or spread, it is mandatory to obtain a correct diagnosis since it may represent a radical change in the patient’s life-prognosis. Herein, the main mechanisms of visual loss are described; we also provide a flow chart to approach the clinical management.
Introducción
La pérdida visual es un motivo de consulta que de por sí implica una anamnesis detallada y una extensa exploración por la multiplicidad de causas con similar presentación clínica. Cuando existen antecedentes de enfermedad neoplásica, este manejo se hace más complejo por dos motivos:- Existen unas etiologías específicas que no se contemplan si no existe dicho antecedente, como la toxicidad por agentes quimioterápicos, efectos indeseables de la radioterapia, enfermedad paraneoplásica, etc.
- La pérdida visual puede representar un cambio en el estado oncológico (recidiva, progresión, invasión del sistema nervioso central) relevante en el pronóstico vital del paciente y su tratamiento.
También pueden existir causas frecuentes de pérdida visual, como glaucoma, catarata, degeneración macular, etc. y es crucial diferenciarlas. En el presente trabajo se revisan las causas “especiales” en el contexto clínico de antecedentes de enfermedad maligna antigua o actual, en remisión o activa, y se desarrolla un algoritmo diagnóstico para su identificación y manejo. Se han clasificado de la siguiente manera: invasión de la vía óptica, relacionadas con hipertensión intracraneal, de tipo paraneoplásico, y finalmente yatrógenica por los efectos indeseables de los tratamientos de la neoplasia. Se presentan ejemplos demostrativos.
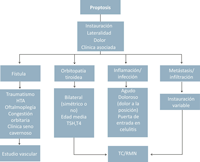
Invasión del aparato o la vía óptica por el tumor
Es el mecanismo más directo y está producido por la presencia física del tumor en algún segmento de la vía óptica. Se pueden diferenciar dos tipos, el compresivo y el infiltrativo.Compresión: el tejido tumoral comprime la vía óptica en cualquier punto desde la órbita hasta el córtex occipital comprometiendo su función. El tumor puede ser originario del mismo punto donde se afecta la vía óptica o ser una extensión de una enfermedad a distancia. Se muestran unos ejemplos en la Figura 1 y la Figura 2.
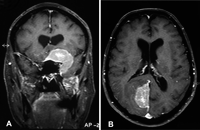
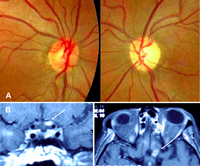
Figura 1. Una paciente de 68 años con antecedentes de neoplasia de mama 14 años antes, consultó por cefalea y pérdida visual en el ojo izquierdo. Se detectó hemianopsia nasal en el ojo derecho y amaurosis en el ojo izquierdo. El estudio de resonancia magnética detectó 2 lesiones con características compatibles con meningioma, sin embargo, la biopsia practicada reveló la presencia de células malignas de iguales características inmuno-histoquímicas que el antiguo tumor primario de mama. Figura 1A. Resonancia magnética cerebral T1 con gadolinio. Corte coronal: Gran lesión en el seno cavernoso izquierdo y vértice de la órbita que invade la fosa temporal y se expande en sentido craneal. Figura 1B. Resonancia magnética cerebral T1 con gadolinio. Corte axial: Lesión en el lóbulo occipital derecho. Ambas presentan realce de la señal tras la administración de gadolinio y comprimen estructuras de la vía visual, una el nervio óptico (amaurosis ojo izquierdo), y la otra el área visual occipital (defecto del campo nasal en el ojo derecho).
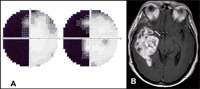
Figura 2. Una paciente de 42 años refirió molestias visuales inespecíficas y dificultades para deambular en las últimas semanas. Dos años atrás se practicó una biopsia estereotáctica para estudiar una lesión intracraneal, compatible con meningioma. Figura 2A. Campo visual. Hemianopsia homónima izquierda. Figura 2B. Resonancia magnética cerebral T1 con gadolinio. Corte axial: Lesión de grandes dimensiones en el lóbulo temporal derecho que desplaza las estructuras de la línea media y comprime la cintilla óptica derecha (flecha).
Infiltración: Hay una invasión de los tejidos de la vía óptica como en una metástasis en la coroides, o una infiltración de nervio y el espacio perióptico. Es característico de los tumores hematológicos y de la carcinomatosis meníngea. Puede presentarse como primera manifestación de la enfermedad o bien ser el primer síntoma de recidiva o progresión. En la Figura 3 y Figura 4 se presenta un ejemplo de metástasis en coroides e invasión del nervio óptico respectivamente.
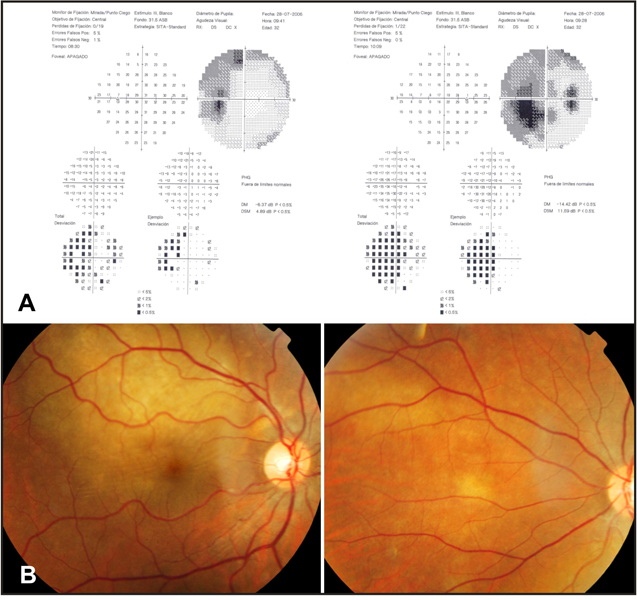
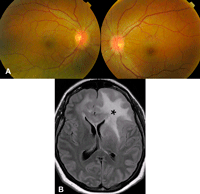
Figura 3. Un joven de 32 años consultó por visión borrosa en el ojo derecho. Tenía antecedentes de adenocarcinoma pleuro-pulmonar y mediastínico con metástasis cervicales activo por lo cual recibía quimioterapia (cisplatino+docitaxel) y radioterapia, El examen del fondo de ojo inicial no mostró alteraciones iniciales, y la campimetría (A). reveló un patrón que sugería una hemianopsia homónima incongruente. El estudio de neuro-imagen no mostró anomalías que comprometieran la vía óptica retroquiasmática. Fondo de ojo (B) En el siguiente control se detectaron lesiones en la coroides de ambos ojos que remedaban el patrón de hemianopsia homónima.
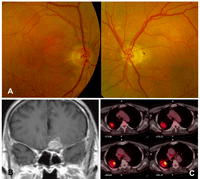
Figura 4. Neuropatía óptica infiltrativa. Paciente fumador de 65 años que consultó por pérdida visual subaguda en el ojo izquierdo, presentaba un defecto pupilar aferente y visión de no percepción luminosa. Figura 4A. Fondo de ojo: Se observó una discreta palidez temporal del disco óptico izquierdo sin elevación ni borramiento de los márgene. Se practicó un estudio de imagen cerebral por sospecha de afectación retrobulbar. Figura 4B. Resonancia magnética cerebral coronal T1 con contraste. Se detectó una lesión que comprimía e infiltraba la porción intracraneal del nervio óptico izquierdo. La captación de contraste en otros nervios craneales sugería un proceso meníngeo infiltrativo y múltiple. Figura 4C. Tomografía de emisión de positrones-TC torácico. Reveló la presencia de un nódulo pulmonar hipercaptante compatible con neoplasia pulmonar responsable de una carcinomatosis meníngea.
Hipertensión intracraneal
El aumento de la presión intracraneal puede afectar la función visual, pero sólo cuando produce papiledema. Cuando existe la infiltración del espacio perióptico no hay transmisión de la presión intracraneal al mismo, es el único caso en que puede haber pérdida visual sin papiledema. En las fases más precoces del papiledema (fase de papiledema incipiente y de papiledema desarrollado) los efectos sobre la función visual son reversibles si la hipertensión se resuelve. La agudeza visual y la visión de colores suele estar conservada salvo cuando el edema del disco se extiende a la mácula. Cuando el proceso avanza y hay pérdida axonal por la hipertensión intracraneal mantenida, la pérdida de visual es irreversible y los defectos de campo visual son permanentes. Esto sucede en las fases de papiledema crónico y atrófico. Se muestra un ejemplo asociado a un marcado deterioro visual en la Figura 5. Algunos tumores localizados en la fosa craneal anterior cursan con un síndrome de Foster Kennedy, consistente en atrofia óptica en un ojo (por compresión directa) y papiledema en el otro ojo (por hipertensión intracraneal).Los tumores intracraneales localizados en la fosa posterior son una frecuente causa de papiledema por compresión del acueducto de Silvio, y también la pueden producir tumores adyacentes a las vellosidades aracnoideas, o aquéllos que las invadan, o que compriman los senos venosos durales. Las metástasis cerebrales o el edema cerebral asociado a los tumores con efecto de masa, aumentan el volumen de tejido cerebral y también pueden producir hipertensión intracraneal. La Figura 6 muestra un ejemplo de papiledema incipiente por un tumor con importante efecto masa pero sin afectación de la función visual.
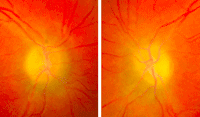
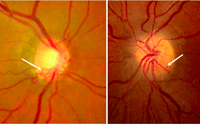
Figura 5. Papiledema atrófico, fondo de ojo: Se aprecian unos discos con márgenes borrosos y palidez difusa. Hay fenómenos de gliosis de los vasos peripapilares.
Figura 6. Papiledema incipiente. Paciente de 40 años con una lesión intracraneal, no presentaba afectación de la agudeza visual, ni discromatopsia, ni alteraciones en el estudio del campo visual. Figura 6A. Fondo de ojo: Se observaba una leve elevación de los discos ópticos en ambos ojos y no había delimitación clara de sus márgenes. Figura 6B. Resonancia magnética cerebral, corte axial T1: La lesión se localizaba en la región fronto-temporal izquierda, se extiendía al cuerpo calloso y a la región frontal izquierda. Provocaba obliteración de las cisternas pre-pedunculares e impronta de las amígdalas cerebelosas en el foramen magno. Estos hallazgos son sugestivos de hipertensión intracraneal.
Paraneoplásica
La mayoría de los síndromes paraneoplásicos están producidos por la secreción tumoral ectópica de hormonas o factores de crecimiento. En el caso de la retinopatía y la neuropatía óptica paraneoplásicas se atribuyen a una reacción inmune cruzada entre antígenos de células neurales normales y las tumorales. Suele ser un diagnóstico de exclusión, y la sospecha se origina por una presentación clínica compatible y la ausencia de lesión sobre la vía óptica por efectos directos del tumor (estudiado con neuroimagen), por agentes infecciosos o por efectos secundarios del tratamiento. Implican un mal pronóstico visual ya que los tratamientos ensayados (esteroides, inmunosupresores, plasmaféresis, etc.) no han demostrado mejoría clínica, y en cuanto al control de la enfermedad maligna, en algunos casos ni siquiera éste consigue revertir o frenar el progreso del deterioro visual.Retinopatía asociada al cáncer-CAR
Es la causa más frecuente de daño visual paraneoplásico. En el 50% de los casos puede preceder al diagnóstico del tumor, cuyas localizaciones más frecuentes son pulmón de tipo célula pequeña, ginecológicas (ovario, endometrio, cérvix) y mama. Las células tumorales expresan proteínas similares a las de la retina externa, contra las cuales se generan auto-anticuerpos. Los anticuerpos anti-recoverina son los más frecuentemente identificados. La destrucción de los fotorreceptores produce una disrupción del impulso nervioso.Los pacientes presentan síntomas sugestivos de disfunción de conos y bastones: fotofobia, deslumbramiento prolongado, pérdida visual y discromatopsia, y escotomas centrales (disfunción de conos) además de ceguera nocturna y adaptación a la oscuridad prolongada con escotomas periféricos o anulares (disfunción de bastones). La exploración del fondo de ojo suele ser normal en fases iniciales, con el tiempo puede aparecer estrechamiento arteriolar, adelgazamiento del epitelio pigmentario de la retina y palidez papilar. Se ilustra con un caso en la Figura 7. Menos frecuentes son las células en vítreo y cámara anterior, envainamiento arteriolar y periflebitis. Las pruebas electrofisiológicas muestran aplanamiento difuso del trazado en condiciones escotópicas y fotópicas. El estudio de anatomía patológica revela la degeneración o pérdida de los fotorreceptores.
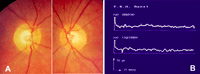
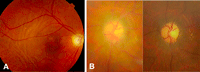
Figura 7. Retinopatía óptica paraneoplásica. Una paciente con antecedentes de neoplasia de mama consultó por marcada pérdida visual bilateral subaguda y fotopsias. La detección de anticuerpos anti-recoverina confirmó el diagnóstico de CAR. Figura 4A. Fondo de ojo: Se aprecia una discreta palidez papilar y atenuación vascular. Figura 4B. Estudio electroretinografía convencional. Hay abolición de la respuesta de los fotorreceptores.
La retinopatía asociada al cáncer debe sospecharse en pacientes con pérdida visual progresiva en contexto de malignidad y fondo de ojo normal o con los sutiles cambios ya descritos, especialmente en las neoplasias pulmonares de célula pequeña (OAT cell). Otras situaciones clínicas a estudiar con electroretinografía (ERG) son: la disfunción de bastones (visión central preservada con contracción de campo visual periférico, fotofobia, nictalopía, estrechamiento arteriolar) y disfunción de conos (pérdida visual, discromatopsia, escotomas centrales), así como fotopsias inexplicadas. En caso de confirmar la disfunción de los fotorreceptores, si no existe historia familiar de distrofia retiniana, es conveniente una evaluación sistémica completa con especial atención a pulmón, mama y pelvis. El líquido cefaloraquídeo puede presentar elevación de las proteínas y linfocitosis. El estudio incluye las determinaciones de los anticuerpos anti-recoverina y antienolasa.
Disfunción de conos asociada al cáncer
Es un subtipo infrecuente de CAR en el que sólo se manifiestan las alteraciones clínicas propias de disfunción de los conos. Estos pacientes consultan por pérdida visual y de visión cromática, y presentan escotomas centrales. Es posible hallar estrechamiento arteriolar y el ERG revela pérdida específica de la actividad de los conos. Recientemente se han descrito alteraciones en la autofluorescencia del fondo consistentes en un anillo hiperfluorescente en la región parafoveal correspondiente a la pérdida de la unión IS/OS y adelgazamiento de la capa nuclear externa.Aunque excepcional, hay que sospechar un efecto remoto del cáncer ante una pérdida visual adquirida inexplicada y disfunción de los conos, sobretodo en ausencia de historia familiar y/o en contexto de sospecha o confirmación de malignidad.
Retinopatía asociada al melanoma -MAR
A diferencia del CAR que puede preceder el diagnóstico de neoplasia, la retinopatía asociada a melanoma suele manifestarse tras una media de 3,6 años en pacientes con historia previa de este tumor cutáneo. En una parte sustancial de los casos descritos, la MAR anuncia la presencia de metástasis no oculares de melanoma. Es más frecuente en hombre que en mujeres y los pacientes refieren fotopsias continuas o intermitentes, pulsátiles e intensas que producen desde leve dificultad en la visión nocturna hasta ceguera y ocasionalmente fotofobia.El inicio puede ser monoocular. Suelen mantener una buena agudeza visual por relativa preservación del campo visual central, y no se afecta la visión cromática. Al igual que en la CAR, el polo posterior suele tener un aspecto normal, aunque con el tiempo puede aparecer estrechamiento arteriolar y palidez papilar.
El ERG muestra una pérdida parcial o completa de la onda B con preservación de la onda A, sobretodo bajo condiciones escotópicas. Estos hallazgos son similares a los de la ceguera nocturna estacionaria congénita y sitúan la disfunción en las células bipolares de la retina. Se han detectado múltiples anticuerpos contra proteínas de diferentes células de la retina pero no se ha identificado el anticuerpo específico contra células bipolares de la retina. Estos hallazgos sugieren un trastorno de autoinmunidad cruzada como causante de la enfermedad.
Se debe sospechar MAR en pacientes con melanoma que desarrollen ceguera nocturna, fotopsias o inexplicable pérdida de campo visual periférico. Una vez establecido el diagnóstico de MAR, es obligada la evaluación sistémica por la correlación entre la aparición de retinopatía paraneoplásica y las metástasis del melanoma. Del mismo modo, los pacientes sin diagnóstico de malignidad pero con afectación clínica y las pruebas compatibles con MAR deben ser examinados por un dermatólogo, es de especial relevancia contemplar la posibilidad de un melanoma oculto en mucosas o en meninges.
Neuropatía óptica paraneoplásica
Mucho menos frecuente que las retinopatías paraneoplásicas, la primera descripción se realizó en un paciente con neoplasia pulmonar de célula pequeña con pérdida visual y ataxia cerebelosa. En la última revisión sobre el tema, solo se habían identificado unos 60 casos, la mayoría en tumores pulmonares de célula pequeña. Otras neoplasias descritas asociadas a la neuropatía óptica paraneoplásica son el linfoma, neuroblastoma, carcinoma papilar de tiroides, carcinoma renal. La pérdida visual aparece de manera bilateral, subaguda, progresiva, e indolora, y progresa en días o semanas. El fondo de ojo puede mostrar edema de papila, ser normal o presentar palidez inicial. En algunos casos se ha descrito exudación vascular periférica y también afectación del quiasma. Se puede detectar en suero los anticuerpos CRMP-5, que también denominan CV2.La mayoría de los casos de neuropatía óptica paraneoplásica aparece en el contexto de múltiples alteraciones neurológicas (signos cerebelosos, disfunción de tronco del encéfalo, demencia subaguda, etc.) El líquido céfalo-raquídeo presenta pleocitosis de predominio linfocítico sin células malignas, elevación de las proteínas, y títulos de IgG anti CRMP-5 iguales o superiores a los del suero.
Relacionadas con el tratamiento de la neoplasia
El deterioro visual puede instaurarse de forma inmediata, de manera diferida precoz o tardíamente tras la remisión de la enfermedad. Las causas se atribuyen a efectos indeseables de la cirugía, de la radioterapia o de la quimioterapia. En algunos casos, 2 o más factores concurren en el mismo paciente.La escisión quirúrgica de un tumor en la vecindad de las estructuras de la vía óptica es uno de los mecanismos de producción (metástasis cerebrales únicas en el lóbulo occipital). La neuropatía óptica bilateral por hipotensión o bajo gasto puede ser una complicación en intervenciones con importante pérdida hemática o hemodilución, aunque este tipo de intervenciones son más frecuentes en cirugía cardíaca o de grandes vasos que en cirugía oncológica.
Radioterapia: Para establecer la plausible toxicidad por radioterapia es preciso investigar qué región ha sido irradiada, las dosis totales y el fraccionamiento, el momento de recibir este tratamiento y correlacionar el intervalo de tiempo entre el tratamiento y la aparición de la pérdida visual. También se debe investigar la presencia de otros factores potenciadores de los efectos indeseables de la radioterapia como quimioterápicos (nitrosureas y vincristina), enfermedades vasculares (diabetes mellitus) o compresión del quiasma (adenomas) Favorece la formación de cataratas, que aparecen tras 2 o 3 años de promedio tras el tratamiento. Cuando las dosis son superiores a 1000cGy invariablemente se desarrolla la catarata radioinducida. Además, las radiaciones ionizantes pueden acelerar los procesos de ateromatosis naturales en el eje carotídeo. Se ha observado la aparición de síndrome de isquemia ocular o episodios de pérdida visual transitoria tipo amaurosis fugax en individuos sometidos a radioterapia cervical.
La retinopatía por radiación aguda aparece al cabo de unos meses y cursa con edema difuso y es autolimitada. Sin embargo, la forma más frecuente se desarrolla entre 6 y 36 meses tras la irradiación y se presenta como microangiopatía vaso-oclusiva por el daño endotelial vascular similar a la retinopatía diabética (Figura 8). Aparecen microaneurismas, hemorragias, exudados blandos y edema macular, incluso puede complicarse con neovascularización, hemovítreo y desprendimiento traccional de retina. La retinopatía es esperable a partir de 4500cGy, el 90% de los casos la presentan con dosis de 7000cGy. Responde a los tratamientos habituales de la diabetes, el papel de los fármacos anti-VEGF se está poniendo a prueba con buenos resultados.
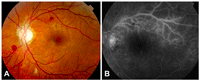
Figura 8. Retinopatía por irradiación. Se realizó tratamiento con radioterapia para un caso de meningioma de la vaina del nervio óptico izquierdo. En un control de rutina de fondo de ojo (A), se detectó la presencia de hemorragias en la retina y exudados blandos. En la angiografía fluoresceínica (B) se observaron alteraciones de la permeabilidad de la pared de los vasos venosos, lo que sugería isquemia de la retina.
La neuropatía por radiación (RON) es un trastorno de tipo isquémico del nervio óptico. Suele ser secundaria a la irradiación de tumores de senos paranasales y de base de cráneo. Para establecer el riesgo de esta complicación son importantes tanto la dosis total como el fraccionamiento. En la mayoría de publicaciones se acepta que por debajo de 50 Gy con fraccionamiento de 2 Gy/ día el riesgo es bajo. Para mayores dosis totales o fraccionamientos superiores aumenta considerablemente la tasa de complicaciones. La máxima incidencia de aparición es alrededor del año tras la radioterapia aunque hay casos descritos entre los 3 meses y los 8 años. La pérdida visual es profunda, indolora y bilateral en el 75 % de los casos. Puede ir precedida de episodios de pérdida visual transitoria unas semanas antes y el deterioro de la función visual progresa en días o semanas. El 85% de los pacientes tienen una agudeza visual final igual o por debajo de 0.1. La forma de presentación más frecuente es la neuropatía óptica posterior, con fondo de ojo normal por afectación de la porción retroocular y evolución a la atrofia óptica en 4-6 semanas (Figura 9). Menos frecuentemente se presenta con edema de papila (neuropatía óptica anterior) que puede asociarse a retinopatía por irradiación.
El diagnóstico diferencial de la neuropatía por radiación se establece entre recurrencia del tumor primario, neoplasia radioinducida y aracnoiditis post irradiación. El estudio con resonancia magnética es obligado para el diagnóstico, que es de exclusión. Por el momento no hay tratamientos que reviertan el deterioro visual, aunque algunos casos y pequeñas series tratados con cámara de oxígeno hiperbárico y esteroides han logrado detener la progresión de la pérdida visual.
Quimioterápicos: Se distinguen los que producen efectos secundarios de manera precoz o a largo plazo. La toxicidad aguda sobre el sistema nervioso es menos frecuente que en otros órganos, tejidos o sistemas por el bajo índice replicativo de las células neuronales y gliales, y por la presencia de la barrera hematoencefálica. La toxicidad neurológica a largo plazo es más frecuente y comportan un mayor riesgo los casos tratados por vía intraarterial. La afectación de la función visual se ha descrito por diferentes mecanismos en diversos fármacos. Las cortas series, el poco seguimiento disponible, la administración habitual de varios fármacos simultáneos y otros factores hacen difícil atribuir determinados efectos secundarios visuales a fármacos en concreto.
- Fludarabina: empleada sobretodo en neoplasias hematológicas poco agresivas (Waldeström, leucemia linfocítica crónica). Se ha descrito cierta frecuencia de pérdida visual, atribuida sobretodo a papilitis a altas dosis del fármaco.
- Nitrosureas: causa grave toxicidad por isquemia neurorretiniana hasta en el 70% de los pacientes semanas tras de su administración intracarotídea. Se sugiere el daño endovascular corio-retiniano como responsable
- Cisplatino: la toxicidad ocular es dosis-dependiente. Hasta el 62% de los pacientes han presentado visión borrosa, pérdida de la sensibilidad cromática o alteraciones del campo visual central junto con alteraciones inespecíficas en el fondo del ojo (pigmentación macular y atrofia del EPR) que son permanentes. La ceguera cortical transitoria es una complicación frecuente del tratamiento con cisplatino, con o sin encefalopatía acompañante. Se han propuesto como mecanismos la desmielinización por toxicidad por metal pesado, la isquemia o la hipomagnesemia por daño tubular. Esta complicación suele ser reversible. También se ha objetivado disfunción del nervio óptico en pacientes tratados con cisplatino. Aunque en ocasiones ha sido referida como neuritis no existe evidencia de causa inflamatoria, así que la denominación más aceptada es neuropatia tóxica. El papiledema y edema de papila han sido descritos en unos pocos casos.
- Vincristina: se une a la tubulina y detiene la mitosis celular. Causa neuropatía óptica no dosis dependiente, a diferencia de la neuropatía periférica en la que también está implicada. Los pacientes que reciben radioterapia y otros quimioterápicos son especialmente susceptibles de desarrollar toxicidad por vincristina. La visión suele mejorar si se discontinúa este fármaco aunque se ha descrito amaurosis irreversible, también se ha implicado en casos de ceguera cortical transitoria.
- Tamoxifeno: causa retinopatía con depósitos maculares cristalinos y edema macular hasta en un 6% de pacientes según las series. El daño retiniano es reversible a bajas dosis, mientras que suele ser persistente en los casos tratados con altas dosis. Se han descrito dos casos de pérdida visual con edema de papila en pacientes que se recuperaron tras la suspensión del fármaco.
- Corticosteroides: el efecto ocular más frecuente son las cataratas uni o bilaterales, que suelen aparecer al cabo de 1 año de tratamiento con dosis por encima de 10mg al día. También causa hipertensión intracraneal (pseudotumor cerebri) en pacientes con cambios recientes en la dosis de corticosteroides tras un largo tiempo recibiéndolos (media 2,5 años)
- Modificadores de la respuesta biológica (incluyen interferones, anti-TNF o interleuquinas): la retinopatía vaso-oclusiva es relativamente frecuente en pacientes tratados con alfa-interferón, aunque es asintomática. Se sospecha la causa isquémica por depósito de inmunocomplejos. Existen casos aislados de neuropatía óptica por interferón (etiquetados de papiledema, papilitis, neuritis óptica y neuropatía óptica isquémica anterior) Se ha descrito la interleuquina 2 como causante de episodios de pérdida visual transitoria y de pérdida transitoria del campo visual, de minutos a horas que desaparecieron al finalizar el tratamiento.
Investigación
Una vez, desarrolladas las principales causas de pérdida de la función visual se detalla el manejo diagnóstico. En primer lugar, afinar con un interrogatorio extenso y dirigido:- Tipo de pérdida: visión borrosa o desenfocada, dificultades para leer, pérdida de campo visual central o periférico, visión doble monocular
- Tiempo de evolución y modo de instauración: aguda (súbita o brusca), subaguda o crónica (lenta y progresiva)
- Lateralidad o localización del proceso (uniocular o ambos ojos): en caso de procesos bilaterales, definir si la presentación es secuencial o simultánea.
- Síntomas acompañantes (cefalea, diplopía, pérdida visual transitoria en relación con la posición de la mirada, defectos de campo visual): en caso de hipertensión intracraneal coexistente, la parálisis de los nervios motores oculares no tiene valor localizador, pero con antecedentes de neoplasia es obligado descartar la compresión, o infiltración de los nervios craneales. La afectación combinada de varios nervios motores oculares sugiere algunas localizaciones anatómicas como el seno cavernoso, o el ápex orbitario, a confirmar con el estudio neuro-radiológico pertinente. En cuanto a los defectos de campo visual existen algunos patrones con valor localizador. La hemianopsia bitemporal sugiere afectación del quiasma óptico, pero la hemianopsia homónima indica una lesión en cualquier localización retroquiasmática. Solo si coexiste defecto pupilar aferente, es sugestivo de afectación de la cintilla óptica, o si hay respeto macular en el lóbulo occipital.
Unos signos o hallazgos clínicos en la exploración tienen una relevancia en cuanto al manejo específico:
- Edema de papila unilateral o bilateral: el estudio del líquido cefaloraquídeo permite detectar aumento de la presión intracraneal en caso de papiledema. La presencia de células malignas sugiere carcinomatosis meníngea.
- Colaterales óptico-ciliares: traduce la afectación en la órbita por compresión crónica del nervio óptico y de la vena central de la retina. La restricción crónica del drenaje de la vena central de la retina que favorecería la apertura de estas vías de drenaje alternativas hacia la circulación coroidea. También aparece en las fases atróficas de papiledema de larga evolución (Figura 10).
- Pliegues coroideos: se observan en dos circunstancias en el contexto de paciente neoplásico, ambas asociadas a compresión del polo posterior (Figura 11). Una es la de tumor o masa que deforma el polo posterior del globo ocular, la otra es la que aparece en la hipertensión intracraneal incluso cuando el papiledema ha resuelto bien por curación, bien por atrofia. Otras posibles causas son escleritis posterior, síndromes inflamatorios orbitarios e hipotensión ocular.
- Proptosis/ enoftalmos: inicialmente puede ser sutil, lo que se aconseja revisar fotografías antiguas aportadas por el paciente. Suele estar relacionada con enfermedad orbitaria, hay proptosis axial cuando se halla ocupación orbitaria por dentro del cono muscular. Aunque infrecuente, el enoftalmos en un paciente con antecedentes de neoplasia es muy sugestivo de enfermedad metastásica del carcinoma fibrosante (escirro) de mama.
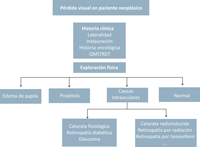
A continuación se presentan los algoritmos diagnósticos para el manejo de la situación de pérdida visual aislada con fondo normal, con alteraciones en la exploración ocular y asociada a proptosis (Tabla 1, Tabla 2, Tabla 3 y Tabla 4).
Tabla 1. Tras la anamnesis dirigida se practica la exploración ocular que puede revelar anomalías como edema de papila, proptosis, o bien ser estrictamente normal. En estas circunstancias, se seguirán las indicaciones de las tablas 2, 3, 4. En otras ocasiones, es posible establecer la causa de la pérdida visual mediante la exploración ocular. Entre las causas oculares se distinguen las comunes y las especiales en el contexto de paciente con antecedentes de neoplasia.
Tabla 2. Algoritmo diagnóstico en caso de proptosis en paciente neoplásico. Si se orienta como causa vascular (tipo fístula) por los antecedentes o hallazgos clínicos, el estudio de imagen se centra en valorar el árbol vascular cerebral. Los estudios apropiados son angio-TC o angioRM. La arteriografía se reserva para los casos tributarios de tratamiento endovascular o cuando no se ha podido confirmar la fístula en las pruebas menos invasivas. Si la sospecha clínica sugiere que hay una lesión ocupante de espacio en la órbita, el estudio de imagen puede revelar alteraciones de los tejidos blandos (grasa, músculo) en la resonancia o bien del hueso en la TC.
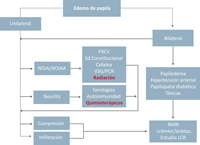
Tabla 3. Algoritmo diagnóstico en caso de edema de papila. Cuando el edema de papila es unilateral y se acompaña de pérdida visual el diagnóstico diferencial se realiza entre las causas isquémicas -neuropatía isquémica arterítica (NOIAA) y no arterítica (NOIA)-, las inflamaciones (neuritis) y las compresivas e infiltrativas. Cuando la presentación es bilateral, aparte de las ya mencionadas, se añaden las causas tóxicas, el papiledema, la neuroretinopatía hipertensiva y la papilopatía diabética. Aparte de las analiticas, serologías y estudios de imagen, es básico determinar la tensión arterial y la glicemia.
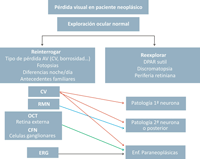
Tabla 4. Algoritmo diagnóstico en caso de fondo de ojo normal. Cuando el examen ocular, especialmente el fondo de ojo, no presenta anomalías, es recomendable reiniciar la anamnesis y repetir la exploración. El estudio del campo visual debe repetirse si los parámetros de confiabilidad son bajos. El patrón de hemianopsia bitemporal y homónima indica que la afectación se encuentra en el quiasma o en vía óptica retroquiasmática, con lo que la neuro-imagen es precisa. Si aparecen nuevos detalles que sugieran una enfermedad paraneoplásica, las pruebas más útiles son el ERG y la OCT de alta resolución. No es infrecuente que antes de realizar el diagnóstico de retinopatía paraneoplásica se haya practicado el estudio de resonancia cerebral, pues la causa infiltrativa o compresiva puede debutar con fondo de ojo normal, y como se indicó las enfermedades paraneoplásicas son “a distancia” y un diagnóstico de exclusión.
Blibliografía
- Walsh FB, Hoyt WF. Clinical Neuro-Ophthalmology. Ed 6, ch 7. 2007, Baltimore, Lippincott. Williams & Wilkins
- Lepore FE. False and non-localizing signs in neuro-ophthalmology. Curr Opin Ophthalmol. 2002;13:371-4
- Castillo BV Jr, Kaufman L. Pediatric tumors of the eye and orbit. Pediatr Clin North Am. 2003;50:149-72.
- Arruga Ginebreda J, Sánchez Dalmau B editores. Neuropatías ópticas: diagnóstico y tratamiento. Madrid: Sociedad Española de Oftalmología; 2002
- Rahimi E, Sarraf D, Paraneoplastic and non-paraneoplastic retinopathy and optic neuropathy: evaluation and management. Surv Ophthalmol. 2013;58:430-58.
- Arruga J. Lesiones metastásicas y paraneoplásicas del nervio óptico. Rev Neurol. 2000;31:1256-8.
- Muñoz S, Martin N, Arruga J. Radiation optic neuropathy treated with hyperbaric oxygen and steroids: stabilization after late treatment. Neuro-Ophthalmol. 2004;28:259-64.