Volumen 21 - Número 5 - Diciembre 2013
Melanoma uveal: anatomía patológica
MA. Saornil Ãlvarez1, M. Quintana Casany2
1Unidad Tumores Intraoculares del Adulto CSUR del SNS.
Hospital Clínico Universitario. Valladolid
2Servicio de Oftalmología. ExJefe de Servicio. Hospital Universitario de Bellvitge. L’Hospitalet de Llobregat (Barcelona)
Hospital Clínico Universitario. Valladolid
2Servicio de Oftalmología. ExJefe de Servicio. Hospital Universitario de Bellvitge. L’Hospitalet de Llobregat (Barcelona)
CORRESPONDENCIA
MA. Saornil
E-mail: saornil@ono.com
E-mail: saornil@ono.com
La histopatología ha desempeñado un papel importante a lo largo de las últimas décadas del siglo XX, tanto en el diagnóstico como en el conocimiento de factores pronósticos y del comportamiento biológico del melanoma de la úvea (McLean 1995, McLean 2004, Font 2006). Actualmente, la gran precisión diagnóstica clínica, mayor del 99%, (COMS report nº 6, 1998) hace que no sea necesario realizar una biopsia para el diagnóstico de esta neoplasia, pero sin embargo se plantea su realización para el conocimiento de factores pronósticos en relación con la supervivencia del paciente (Damato 2011).
Los melanomas se originan en los melanocitos de la úvea y suelen comenzar como nódulos coroideos asintomáticos (Figura 1) que, al crecer, pueden romper la membrana de Bruch y adquirir una forma de champiñón, levantando e invadiendo la retina (Figura 2). Si el tumor sigue creciendo, puede invadir otras estructuras oculares como el cuerpo ciliar (factor de mal pronóstico), empujar el cristalino e invadir la cámara anterior, pudiendo producir glaucoma secundario (Bianciotto 2005) (Figura 3), o llenar por completo el globo ocular o extenderse fuera de él, lo cual empeora notablemente el pronóstico vital del paciente (Blanco 2004).
El tamaño del melanoma y la localización o invasión del cuerpo ciliar son dos importantes factores pronósticos que deben tenerse en cuenta en la evaluación de los melanomas, tanto en el estudio macroscópico como en el microscópico. Aunque los oftalmólogos suelen utilizar ambos diámetros, base y altura, para clasificar el tamaño, los patólogos generalmente usan una clasificación simple basada en el mayor diámetro tumoral, dividiendo los melanomas en (McLean 1995, McLean 2004):
El tipo celular es uno de los indicadores pronósticos más fiables. Según la modificación de la clasificación de Callender de 1931 (Callender 1931), realizada por McLean et al. en 1983 (McLean 1983) de demostrado valor pronóstico, los tipos celulares que pueden encontrarse en los melanomas de la úvea son (Figura 4):
El pronóstico del paciente se encuentra en relación directa con la presencia de células epitelioides que componen el tumor: cuanta mayor proporción, peor supervivencia (McLean 2004, Damato 2011).
Las células melanocíticas, y por lo tanto las que componen los melanomas, expresan las proteínas S100, HMB45 y Melan A, que se detectan por inmunohistoquímica y son útiles en el diagnóstico diferencial de tumores indiferenciados para esclarecer su origen (Burnier 1991, Fernandes 2007) (Figura 5).
La esclera se comporta como una barrera para el crecimiento del melanoma uveal, por lo que su extensión extraocular suele ocurrir a través de los canales emisarios de las venas vorticosas y de los vasos ciliares. En ocasiones las células pueden invadir la luz de las venas vorticosas o el nervio óptico, aunque con poca frecuencia se extienden más allá de la lámina cribosa. De cualquier forma que el tumor alcance la superficie ocular, lo que empeora la evolución y el pronóstico del paciente es el hecho de que células tumorales alcancen los tejidos de la órbita (Blanco 2004) (Figura 6 y Figura 7).
La actividad proliferativa tumoral puede medirse contando el número de mitosis por campo de gran aumento o mediante técnicas de inmunohistoquímica, método más objetivo y preciso de medir la proliferación. Los anticuerpos monoclonales para Ki-67/Mib-1 y PCNA han demostrado ser un parámetro con valor pronóstico independiente para el melanoma de úvea (Mooy 1996) (Figura 8 y Figura 9).
Folberg et al. (1993) demostraron el valor pronóstico de ciertos patrones vasculares, como la presencia de lazos vasculares y patrones en red (asas cerradas contiguas) que presentan una gran correlación con una menor supervivencia del paciente (Figura 10).
La infiltración linfocitaria, predominantemente de linfocitos T, se encuentra sólo en el 5% al 12% de los melanomas de úvea, y se asocia a un incremento de la mortalidad por metástasis (Figura 11). Se ha sugerido que esto ocurre porque es necesaria la diseminación de células tumorales en el melanoma de coroides para que se genere una respuesta mediada por linfocitos T (Whelchel 1993). La presencia de macrófagos es más común, y pueden detectarse mediante técnicas de inmunohistoquímica utilizando anticuerpos anti-CD68; su presencia es mayor en los tumores grandes y con células epitelioides, y por lo tanto de peor pronóstico (Makitie 2001).
Estudios citogenéticos recientes han demostrado que la monosomía en el cromosoma 3 es un valioso marcador pronóstico que empeora cuando, además, aparecen copias adicionales del cromosoma 8, y monosomía del cromosoma 1 (Damato 2007, Damato 2011).
Todos estos factores histopatológicos y citogenéticos no son independientes, por lo que los análisis multivariados han demostrado que los tumores grandes suelen invadir el cuerpo ciliar, contener una elevada proporción de células epitelioides, tender a la extensión extraescleral y presentar anomalías en los cromosomas 3 y 8, asociándose los factores de mal pronóstico.Teniendo en cuenta esta interrelación se ha realizado la última revisión de la clasificación TNM (Kivela 2013) y también se han desarrollado modelos predictivos para ajustar con la mayor precisión posible el pronóstico de los pacientes (Damato 2011).
Los melanomas se originan en los melanocitos de la úvea y suelen comenzar como nódulos coroideos asintomáticos (Figura 1) que, al crecer, pueden romper la membrana de Bruch y adquirir una forma de champiñón, levantando e invadiendo la retina (Figura 2). Si el tumor sigue creciendo, puede invadir otras estructuras oculares como el cuerpo ciliar (factor de mal pronóstico), empujar el cristalino e invadir la cámara anterior, pudiendo producir glaucoma secundario (Bianciotto 2005) (Figura 3), o llenar por completo el globo ocular o extenderse fuera de él, lo cual empeora notablemente el pronóstico vital del paciente (Blanco 2004).
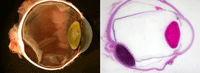
Figura 1. Macroscopia y microscopia óptica de bajo aumento de melanoma nodular.
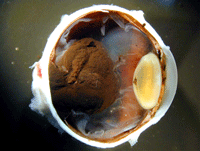
Figura 2. Melanoma en champiñón con invasión de retina y vítreo.
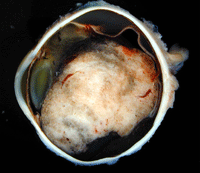
Figura 3. Melanoma grande con invasión de cuerpo ciliar y cámara vítrea que luxa cristalino y cierra el ángulo de la cámara anterior.
El tamaño del melanoma y la localización o invasión del cuerpo ciliar son dos importantes factores pronósticos que deben tenerse en cuenta en la evaluación de los melanomas, tanto en el estudio macroscópico como en el microscópico. Aunque los oftalmólogos suelen utilizar ambos diámetros, base y altura, para clasificar el tamaño, los patólogos generalmente usan una clasificación simple basada en el mayor diámetro tumoral, dividiendo los melanomas en (McLean 1995, McLean 2004):
- Pequeños: ≤ 10mm (supervivencia a 20 años del78%).
- Medianos: 11-15 mm (supervivencia a 20 años del55%).
- Grandes: ≥ 15mm (supervivencia a 20 años del30%)
El tipo celular es uno de los indicadores pronósticos más fiables. Según la modificación de la clasificación de Callender de 1931 (Callender 1931), realizada por McLean et al. en 1983 (McLean 1983) de demostrado valor pronóstico, los tipos celulares que pueden encontrarse en los melanomas de la úvea son (Figura 4):
- Células fusiformes A: núcleo fusiforme homogéneo con pliegue longitudinal, cromatina fina y nucléolo indistinguible.
- Células fusiformes B: núcleo ovoideo, cromatina en acúmulos y nucléolo prominente.
- Células epitelioides: más grandes, redondeadas o poliédricas, con citoplasma abundante y borde celular bien definido. El núcleo es redondeado, grande y con un nucléolo grande eosinófilo en el centro.
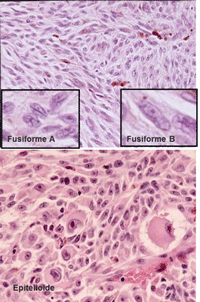
Figura 4. Tipos de células de melanoma.
El pronóstico del paciente se encuentra en relación directa con la presencia de células epitelioides que componen el tumor: cuanta mayor proporción, peor supervivencia (McLean 2004, Damato 2011).
Las células melanocíticas, y por lo tanto las que componen los melanomas, expresan las proteínas S100, HMB45 y Melan A, que se detectan por inmunohistoquímica y son útiles en el diagnóstico diferencial de tumores indiferenciados para esclarecer su origen (Burnier 1991, Fernandes 2007) (Figura 5).
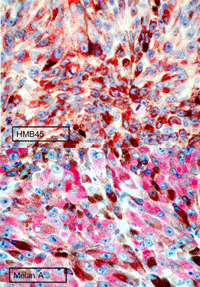
Figura 5. Immunohistoquímica HMB45 y Melan A.
La esclera se comporta como una barrera para el crecimiento del melanoma uveal, por lo que su extensión extraocular suele ocurrir a través de los canales emisarios de las venas vorticosas y de los vasos ciliares. En ocasiones las células pueden invadir la luz de las venas vorticosas o el nervio óptico, aunque con poca frecuencia se extienden más allá de la lámina cribosa. De cualquier forma que el tumor alcance la superficie ocular, lo que empeora la evolución y el pronóstico del paciente es el hecho de que células tumorales alcancen los tejidos de la órbita (Blanco 2004) (Figura 6 y Figura 7).
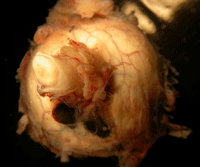
Figura 6. Extensión extraocular a través de canales emisarios ciliares cortos posteriores.
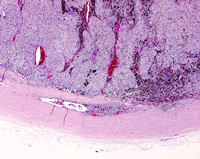
Figura 7. H&E x10: extensión escleral perivascular a través de canal emisario.
La actividad proliferativa tumoral puede medirse contando el número de mitosis por campo de gran aumento o mediante técnicas de inmunohistoquímica, método más objetivo y preciso de medir la proliferación. Los anticuerpos monoclonales para Ki-67/Mib-1 y PCNA han demostrado ser un parámetro con valor pronóstico independiente para el melanoma de úvea (Mooy 1996) (Figura 8 y Figura 9).
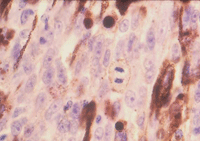
Figura 8. H&E x40: mitosis melanoma.
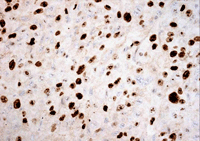
Figura 9. Ki67 x 40 Mib-1: índice proliferativo mayor del 25%.
Folberg et al. (1993) demostraron el valor pronóstico de ciertos patrones vasculares, como la presencia de lazos vasculares y patrones en red (asas cerradas contiguas) que presentan una gran correlación con una menor supervivencia del paciente (Figura 10).
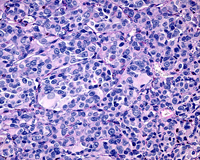
Figura 10. PAS x 40: patrón vascular en red con más de tres asas cerradas contiguas.
La infiltración linfocitaria, predominantemente de linfocitos T, se encuentra sólo en el 5% al 12% de los melanomas de úvea, y se asocia a un incremento de la mortalidad por metástasis (Figura 11). Se ha sugerido que esto ocurre porque es necesaria la diseminación de células tumorales en el melanoma de coroides para que se genere una respuesta mediada por linfocitos T (Whelchel 1993). La presencia de macrófagos es más común, y pueden detectarse mediante técnicas de inmunohistoquímica utilizando anticuerpos anti-CD68; su presencia es mayor en los tumores grandes y con células epitelioides, y por lo tanto de peor pronóstico (Makitie 2001).
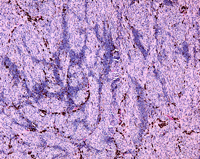
Figura 11. H&E x 20: infiltrado linfocitario en melanoma uveal.
Estudios citogenéticos recientes han demostrado que la monosomía en el cromosoma 3 es un valioso marcador pronóstico que empeora cuando, además, aparecen copias adicionales del cromosoma 8, y monosomía del cromosoma 1 (Damato 2007, Damato 2011).
Todos estos factores histopatológicos y citogenéticos no son independientes, por lo que los análisis multivariados han demostrado que los tumores grandes suelen invadir el cuerpo ciliar, contener una elevada proporción de células epitelioides, tender a la extensión extraescleral y presentar anomalías en los cromosomas 3 y 8, asociándose los factores de mal pronóstico.Teniendo en cuenta esta interrelación se ha realizado la última revisión de la clasificación TNM (Kivela 2013) y también se han desarrollado modelos predictivos para ajustar con la mayor precisión posible el pronóstico de los pacientes (Damato 2011).
Bibliografía recomendada
- Bianciotto C, Saornil MA, Muiños Y, Méndez MC, Blanco G, Frutos-Baraja JM, et al. Hipertensión ocular como principal forma de presentación del melanoma uveal. Arch Soc Esp Oftalmol. 2005;80:27-34.
- Blanco G. Diagnosis and treatment of orbital invasion in uveal melanoma. Can J Ophthalmol. 2004;39:388-96.
- Burnier MN, McLean IW, Gamel JW. Immunohistochemical evaluation of uveal melanocytic tumors. Expression of HBM-45, S-100 protein, and neuron-specific enolase. Cancer. 1991;68:809-14.
- Callender GR. Malignant melanotic tumors of the eye: a study of histologic types in 111 cases. Trans Am Acad Ophthalmol Otolaryngol. 1931;36:131-42.
- COMS report nº6. Histopathologic characteristics of uveal melanomas in eyes enucleated from the Collaborative Ocular Melanoma Study. Am J Ophthalmol. 1998;125:745-66.
- Damato B, Duke C, Coupland SE, Hiscott P, Smith PA, Campbell I, et al. Cytogenetics of uveal melanoma: a 7-year clinical experience. Ophthalmology. 2007;114:1925-31.
- Damato B, Coupland SE.A reappraisal of the significance of largest basal diameter of posterior uveal melanoma. Eye. 2009;23:2152-60.
- Damato B, Eleuteri A, TakTak A, Coupland SE. Estimating prognosis for survival after treatment of choroidal melanoma. Prog Retin Eye Res. 2011;30:285-95.
- Fernandes BF, Odashiro AN, Saraiva VS, Logan P, Antecka E, Burnier MN Jr. Immunohistochemical expression of melan-A and tyrosinasi in uveal melanoma. J Carcinog. 2007;20:6.
- Folberg R, Rummelt V, Parys-Van Ginderdeuren R, Hwang T, Woolson RF, Pe’er J, et al. The prognostic value of tumor blood vessel morphology in primary uveal melanoma. Ophthalmology. 1993;100:1389-98.
- Font RL. Tumors ofthe uveal tract. En: Font RL, Croxatto JO, Rao NA, eds. Tumors of the Eye and Ocular Adnexa. AFIP Atlas of Tumor Pathology. Series4. Washington: AFIP;2006.p.41-79.
- Kivela T, Kujala E. Prognostication in eye cancer: the latests Tumor, Node, Metastasis classification and beyond. Eye. 2013;27:243-52.
- Makitie T, Summanen P, Tarkkanen A, Kivela T. Tumor-infiltrating macrophages (CD68(+) cells) and prognosis in malignantuveal melanoma. Invest Ophtalmol Vis Sci. 2001;42:1414-21.
- McLean IW, Foster WD, Zimmerman LE, Gamel JW. Modifications of Callender’s classification of uveal melanoma at the Armed Forces Institute of Pathology. Am J Ophthalmol. 1983;96:502-9.
- McLean IW. Prognostic features of uveal malignant melanoma.Ophthalmol Clin North Am. 1995;8:143-53.
- McLean IW, Saraiva VS, Burnier MN Jr. Pathological and prognostic features of uveal melanomas. Can J Ophthalmol. 2004;39:343-50.
- Mooy CM, De Jong PT. Prognostic parameters in uveal melanoma: a review. Surv Ophthalmol. 1996;41:215-28.
- Whelchel JC, Farah SE, McLean IW, Burnier MN. Immunohistochemistry of infiltrating lymphocytes in uveal malignant melanoma. Invest Ophtalmol Vis Sci. 1993;34:2603-6.