Volumen 21 - Número 2 - Junio 2013
Neuroconducta del prematuro tras exploración oftalmológica
Ã. Arranz-Betegón1, S. Parés-Tercero1, E. Sánchez Ortiz1, G. Freixas Orellana1, J. Navarro-Segarra2, A. Fornieles-Deu3, C. Costas-Moragas4, F. Botet1
1Servei de Neonatología (ICGON), Hospital Clínic de Barcelona. Universitat de Barcelona. IDIBAPS
2Laboratorio de referencia de Cataluña
3Departament de Psicobiologia i Metodologia de les Ciències de la Salut. Facultat de Psicologia. Universitat Autònoma de Barcelona
4Departament de Psicologia Clínica i de la Salut. Facultat de Psicologia. Universitat Autònoma de Barcelona
2Laboratorio de referencia de Cataluña
3Departament de Psicobiologia i Metodologia de les Ciències de la Salut. Facultat de Psicologia. Universitat Autònoma de Barcelona
4Departament de Psicologia Clínica i de la Salut. Facultat de Psicologia. Universitat Autònoma de Barcelona
CORRESPONDENCIA
Ángela Arranz-Betegón
Servei de Neonatología (ICGON), Hospital Clínic de Barcelona
Universitat de Barcelona. IDIBAPS
Sabino de Arana, 1. 08028 Barcelona
E-mail: aarranz@clinic.ub.es
Servei de Neonatología (ICGON), Hospital Clínic de Barcelona
Universitat de Barcelona. IDIBAPS
Sabino de Arana, 1. 08028 Barcelona
E-mail: aarranz@clinic.ub.es
RESUMEN
Objetivos: Evaluar los cambios neuroconductuales en prematuros después de la exploración oftalmológica.
Pacientes y métodos: Estudio prospectivo casos-control. Catorce bebés prematuros (33 semanas) en situación hemodinámica estable fueron sometidos a una exploración oftalmológica. Se utilizó una adaptación de la pauta de observación neuroconductual NIDCAP (Newborn Individualized Development Care and Assessment Program) entre 12 y 18 horas tras la exploración. Los períodos de observación fueron: 1) periodo basal 2) en el episodio de un cuidado (cambio de pañales) y 3) fase de recuperación. El grupo control contenía 60 recién nacidos prematuros.
Resultados: Se detectaron diferencias significativas en los prematuros del grupo de estudio entre la línea de base y la fase de recuperación en 6 señales de estrés. En el "cambio de pañales" (fase 3), las señales de estrés fueron observadas con frecuencias significativamente mayores en el grupo de estudio. Éstas pertenecen al sistema autónomo (respiración irregular, sonidos de queja indiferenciada, sobresaltos, hipo y temblores).
Conclusión: Los resultados sugieren que la exploración oftalmológica en los bebés prematuros ejerce un efecto negativo en su organización neuroconductual. Es aconsejable cubrir la incubadora para reducir el período de manipulación.
Pacientes y métodos: Estudio prospectivo casos-control. Catorce bebés prematuros (33 semanas) en situación hemodinámica estable fueron sometidos a una exploración oftalmológica. Se utilizó una adaptación de la pauta de observación neuroconductual NIDCAP (Newborn Individualized Development Care and Assessment Program) entre 12 y 18 horas tras la exploración. Los períodos de observación fueron: 1) periodo basal 2) en el episodio de un cuidado (cambio de pañales) y 3) fase de recuperación. El grupo control contenía 60 recién nacidos prematuros.
Resultados: Se detectaron diferencias significativas en los prematuros del grupo de estudio entre la línea de base y la fase de recuperación en 6 señales de estrés. En el "cambio de pañales" (fase 3), las señales de estrés fueron observadas con frecuencias significativamente mayores en el grupo de estudio. Éstas pertenecen al sistema autónomo (respiración irregular, sonidos de queja indiferenciada, sobresaltos, hipo y temblores).
Conclusión: Los resultados sugieren que la exploración oftalmológica en los bebés prematuros ejerce un efecto negativo en su organización neuroconductual. Es aconsejable cubrir la incubadora para reducir el período de manipulación.
RESUM
Objectius: Avaluar els canvis neuroconductuals en nadons prematurs després de l'exploració oftalmològica.
Pacients i mètodes: Estudi prospectiu de casos i grup control. Catorze nadons prematurs (33 setmanes) amb situació hemodinàmica estable van ser sotmesos a una exploració oftalmològica. Es va utilitzar una adaptació de la pauta d’observació neuroconductual NIDCAP (Newborn Individualized Development Care and Assessment Program) entre les 12-18 hores posteriors a l'exploració oftalmològica. Els períodes d'observació van ser: 1) període basal 2) durant l’episodi d'una cura (canvi de bolquers) i 3) fase de recuperació. El grup control contenia 60 nounats prematurs.
Resultats: Es van detectar diferències significatives en 6 senyals d'estrès en els nadons en el grup d'estudi entre la línia de base i la fase de recuperació. Durant el “canvi de bolquers” (fase 3), els senyals d'estrès van ser observats amb freqüències significativament majors en el grup d'estudi. Aquests pertanyen al sistema autònom (respiració irregular, sons de queixa indiferenciats, sobresalts, sanglot i tremolors).
Conclusió: Els resultats suggereixen que l'exploració oftalmològica en els nadons prematurs té efectes negatius en la seva organització neuroconductual. És aconsellable cobrir la incubadora per reduir el període de manipulació.
Pacients i mètodes: Estudi prospectiu de casos i grup control. Catorze nadons prematurs (33 setmanes) amb situació hemodinàmica estable van ser sotmesos a una exploració oftalmològica. Es va utilitzar una adaptació de la pauta d’observació neuroconductual NIDCAP (Newborn Individualized Development Care and Assessment Program) entre les 12-18 hores posteriors a l'exploració oftalmològica. Els períodes d'observació van ser: 1) període basal 2) durant l’episodi d'una cura (canvi de bolquers) i 3) fase de recuperació. El grup control contenia 60 nounats prematurs.
Resultats: Es van detectar diferències significatives en 6 senyals d'estrès en els nadons en el grup d'estudi entre la línia de base i la fase de recuperació. Durant el “canvi de bolquers” (fase 3), els senyals d'estrès van ser observats amb freqüències significativament majors en el grup d'estudi. Aquests pertanyen al sistema autònom (respiració irregular, sons de queixa indiferenciats, sobresalts, sanglot i tremolors).
Conclusió: Els resultats suggereixen que l'exploració oftalmològica en els nadons prematurs té efectes negatius en la seva organització neuroconductual. És aconsellable cobrir la incubadora per reduir el període de manipulació.
ABSTRACT
Objectives: To evaluate neurobehavioral changes in premature infants after ophthalmological exploration.
Patients and methods: Prospective cohort study. Fourteen premature infants (33 weeks) underwent ophthalmologic exploration. The control group contained 60 premature infants. Only premature infants in a stable homodynamic situation were included. An adaptation of the neurobehavioral observation suggested by NIDCAP–Sheet (Newborn Individualized Development Care and Assessment Program) was used between 12 and 18 hours after ophthalmologic exploration. The observation periods were: 1) baseline 2) care-giving episode (diaper-changing) and 3) recovery phase.
Results: In the “baseline” and “recovery” phases, the neonates in the study group obtained significant differences in 6 stress signals. In the “diaper-changing” phase, 3 stress signals were observed at significantly greater frequencies in the study group. The stress signals observed belong to the autonomic system (irregular respiration, undifferentiated whimper-like sounds, startles, hiccoughs, and tremors).
Conclusion: The results obtained provide data on the negative effects on neurobehavioral organization of premature neonates which could be globally attributed to the ophthalmologic exploration. It is advisable for incubator covers to be put in place, in order to reduce the period of manipulation.
Patients and methods: Prospective cohort study. Fourteen premature infants (33 weeks) underwent ophthalmologic exploration. The control group contained 60 premature infants. Only premature infants in a stable homodynamic situation were included. An adaptation of the neurobehavioral observation suggested by NIDCAP–Sheet (Newborn Individualized Development Care and Assessment Program) was used between 12 and 18 hours after ophthalmologic exploration. The observation periods were: 1) baseline 2) care-giving episode (diaper-changing) and 3) recovery phase.
Results: In the “baseline” and “recovery” phases, the neonates in the study group obtained significant differences in 6 stress signals. In the “diaper-changing” phase, 3 stress signals were observed at significantly greater frequencies in the study group. The stress signals observed belong to the autonomic system (irregular respiration, undifferentiated whimper-like sounds, startles, hiccoughs, and tremors).
Conclusion: The results obtained provide data on the negative effects on neurobehavioral organization of premature neonates which could be globally attributed to the ophthalmologic exploration. It is advisable for incubator covers to be put in place, in order to reduce the period of manipulation.
Introducción
Uno de los problemas sensoriales que presentan los niños prematuros es la retinopatía del prematuro (ROP), potencial causa de ceguera y que se presenta cuando la retina inmadura se desarrolla en un ambiente postnatal adverso. La ceguera debida a la ROP es más frecuente en niños nacidos con menos de 28 semanas y frecuentemente se asocia a otras secuelas de la prematuridad. Según el Center for Disease Control and Prevention (CDC), en 2004, la ROP fue la causa más común de ceguera en niños de cualquier edad.Según las recomendaciones de la American Academy of Pediatrics (AAP) (2006) el cribaje de la ROP debe realizarse sistemáticamente en recién nacidos antes de las 30 semanas o de menos de 1500 gramos. De manera adicional también deben incluirse neonatos entre 1500 a 2000 gramos cuyo curso clínico sea inestable. Los neonatos nacidos antes de la semana 28 deberían someterse a exploración alrededor de las 31 semanas de edad corregida para minimizar el número de exámenes. La importancia de estas exploraciones tempranas deriva del estudio ETROP (Early Treatment for Retinopathy of Prematurity Cooperative Group), realizado en 2005, en el que se demostró que los neonatos que se diagnosticaron y trataron precozmente obtuvieron mejores resultados que los que no se trataron1.
Según el protocolo establecido, la exploración de la ROP se realiza mediante oftalmoscopia binocular sin blefarostato ni indentador (Figura 1), bajo dilatación pupilar con procaína 0,5%, tropicamida 0,5% y fenilefrina 2,5%, instiladas al menos 30 minutos antes del examen (Figura 2). Después de cada gota se comprime el punto lagrimal durante dos minutos para evitar el paso a la mucosa nasal y su posterior absorción sistémica2 (Figura 3). Aunque las complicaciones de los fármacos midriáticos y ciclopléjicos son raras, los efectos adversos suelen estar relacionados con las dosis y otros factores. Las complicaciones oculares incluyen aumento de la presión intraocular, pigmentación de la conjuntiva y de la córnea, pigmentación del segmento anterior del ojo, obstrucción del conducto nasolacrimal, edema macular, daño en el endotelio corneal, hiperemia, alergia, visión borrosa3, pueden derivar directamente de la propia maniobra como por ejemplo la infrecuente hemorragia conjuntival4, del malestar debido al dolor o al estrés, o pueden derivarse de los efectos colaterales de los fármacos utilizados tópicamente cuando se produce su paso a la circulación sistémica, debido a que el recién nacido es más sensible a éstos. En relación a los efectos sistémicos se han descrito: aumento de la presión arterial (sistólica y diastólica)5-9, taquicardia3,8,9, dolor de cabeza, debilidad, palidez, temblor, sudoración profusa, palpitaciones, arritmia, somnolencia, enrojecimiento de la piel, fiebre, sequedad de boca, convulsiones, nerviosismo3, enterocolitis necrotizante10, disminución de la secreción ácida gástrica, íleo (inhibición de la motilidad duodenal, retraso del vaciado gástrico, distensión abdominal, vómitos)11-14, insuficiencia renal15 y fallo cardíaco16. Algunos trabajos han monitorizado también variables de tipo conductual o psicológico como medida del impacto negativo de esta maniobra exploratoria, por ejemplo a través del Premature Infant Pain Profile (PIPP)17-19.
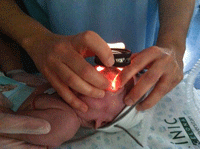
Figura 1. Revisón del fondo de ojo con un oftalmoscopio indirecto.
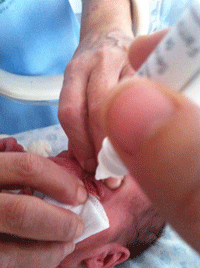
Figura 2. Entre dos enfermeras se realiza la colocación de gotas oftalmológicas.
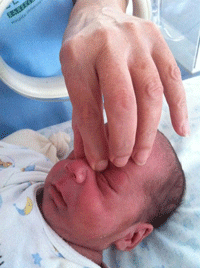
Figura 3. Presión sobre el conducto lacrimal para evitar que el producto pase a circulación sintética.
Se cree que la coparticipación de los diferentes aspectos que comporta la maniobra de exploración oftalmológica (manipulación del ojo, absorción de fármacos instilados) es responsable de la aparición de los diferentes efectos negativos observados17,20-22,23. Esto se evidencia en las diferentes maniobras propuestas para paliar o eliminar dichos efectos y en los diferentes resultados obtenidos. Así, para disminuir las molestias de tipo local derivadas de la manipulación del globo ocular del neonato se utiliza un anestésico local como la proparacaína, si bien el efecto buscado con este anestésico no siempre se logra19,24. También se ha recomendado, sin que haya un acuerdo general, el uso de sacarosa para minimizar el dolor debido a esta maniobra1,25,26. Por otro lado, algunos de los efectos no deseables de tipo farmacológico (alucinaciones, sed, boca seca, confusión, desorientación, nerviosismo, etc.) no son objetivables en el neonato prematuro debido a su propia condición y posiblemente sólo puedan observarse a través de signos indirectos asociados, como los que puedan extraerse de la observación de la esfera neuroconductual17,18. En un reciente estudio realizado por Kleberg, et al.27 se ha detectado que el uso del Newborn Individualized Developmental Care and Assessment Program aplicado a neonatos durante la exploración, se asoció a mejores puntuaciones de comportamiento durante el examen y, aunque no reduce las respuestas ante el dolor, mejora su recuperación posterior.
Tal como se ha expuesto, la mayoría de las investigaciones realizadas hasta ahora se han centrado en el análisis de los efectos fisiológicos producidos por la exploración oftalmológica, así como en las reacciones inmediatas del neonato ante el dolor. Sin embargo, se conocen poco las manifestaciones neuroconductuales que puede provocar dicha maniobra. Con este fin, el objetivo de este estudio es registrar y evaluar los cambios neuroconductuales de los neonatos prematuros de 33 semanas de gestación, sometidos a una exploración oftalmológica sistemática para la detección de la retinopatía del prematuro.
Pacientes y método
El grupo de estudio está compuesto por 14 neonatos prematuros de 33 semanas de edad postmenstrual a los que se les realizó la exploración oftalmológica para la detección de la ROP. Como grupo control de referencia se tomó el perfil neuroconductual de 102 observaciones obtenidas en la semana 33 de edad postmenstrual realizadas en 60 neonatos de las mismas características. Se han incluido recién nacidos en situación hemodinámica estable. Se excluyeron los neonatos que en el momento de la exploración presentaban de forma activa hemorragia intracraneal, sepsis, que recibían en aquel momento fármacos depresores del sistema nervioso central o tratamiento con fototerapia. Se obtuvo el consentimiento informado de los padres y el proyecto fue aprobado por el Comité de Ética del centro.Todos los exámenes fueron realizados por la oftalmóloga habitual, que colabora con el Servicio desde hace 12 años. Las exploraciones se realizaron mediante oftalmoscopia indirecta, en la Unidad de Neonatologia del ICGON (Instituto Clínico Ginecológico Obstétrico y Neonatológico del Hospital Clínic de Barcelona).
Una de las formas de valorar la esfera neuroconductual de los neonatos es mediante el uso de pautas de observación. En este estudio se ha utilizado una adaptación de la pauta de observación del programa NIDCAP (Newborn Individualized Development Care and Assessment Program)21. Esta pauta de observación neuroconductual, si bien fue creada por H. Als para un uso cualitativo e idiográfico, actualmente existen diferentes equipos que la utilizan con una finalidad cuantitativa o nomotética, ya sea en su totalidad o parcialmente con el fin de poder establecer comparaciones inter-sujetos (Goldstein, Holsti, Pressler). La adaptación que hemos utilizado, a la que denominamos Premature Observation Sheet (POS), contiene los mismos ítems que la versión original, con la adición de dos ítems: “Seguimiento visual del neonato de la cara del adulto” y “Atención hacia la voz del adulto”. La POS consta de 83 ítems que se pueden clasificar en signos de estrés o comportamiento desorganizado y signos de estabilidad o conductas de regulación, que se puntúan con 1 o 0. Se agrupan en tres sistemas constituidos por varios subsistemas: el sistema autonómico (respiración, color, patrones motores relacionados con la inestabilidad autonómica y conductas viscerales-respiratorias), el sistema motor (conductas generales de las extremidades y del tronco, movimientos específicos de las extremidades y conductas faciales) y por último el sistema integrado por las conductas relativas al estado de conciencia y a la atención.
Se cuenta con una hoja de registro para un período de 10 minutos de observación. En la pauta hay cinco columnas de registro que son secuencias de 2 minutos cada una. Las observaciones se anotan marcando la presencia de cada conducta durante estos períodos de 2 minutos. Los períodos de observación (10 minutos), son los siguientes: 1) observaciones iniciales (fase basal), en el que se observa al recién nacido antes de que la enfermera o la madre/padre empiece con los cuidados habituales (cambio de pañales, alimentación). El neonato no recibe ninguna estimulación extra ni se le manipula; 2) episodio de cuidado: se observa durante los cuidados (cambio de pañal y alimentación). Se valoran las reacciones del neonato ante tales estímulos y 3) recuperación: se observa justo después de haber dejado al neonato en la incubadora o cuna. El neonato no recibe ninguna estimulación y se valora su capacidad de recuperación. Los neonatos del grupo estudio15 fueron evaluados con la POS entre 12 y 18 horas después de la exploración oftalmológica sistemática para la detección de la retinopatía de la prematuridad. La observación se llevó a cabo siguiendo la pauta mencionada, es decir: 1) Observaciones iniciales 2) en el episodio de cuidado y 3) en la recuperación.
Con el fin de obtener un perfil neuroconductual esperable del neonato prematuro de 33 semanas de edad gestacional, la misma pauta POS se administró a los 60 neonatos del grupo control, equiparables, tanto por su edad gestacional como por los parámetros fisiológicos, al grupo estudio. En este caso, los tres momentos de observación fueron también los convencionales, pero en esto caso los neonatos no habían sido sometidos a ningún examen oftalmológico. Todas las observaciones fueron realizadas por 7 examinadores entrenados, los cuales habían obtenido una fiabilidad interevaluadores entre 90% y 100% con el coordinador de la investigación. Los examinadores que realizaron las observaciones desconocían totalmente el objetivo del estudio, por lo que ignoraban si a los niños que observaban se les había realizado o no la exploración oftalmológica.
Para realizar el tratamiento estadístico de los datos se utilizaron los programas Microsoft Excel y Statistical Package for Social Sciences (SPSS 15.0). En el análisis de los resultados se utilizó como indicador estadístico la frecuencia de presentación de los diferentes ítems, calculando también la Odds ratio (razón de oportunidades) de cada ítem. La razón de Odds Ratios (OR) de la exposición puede interpretarse como un indicador indirecto del riesgo de sufrir el síntoma.
Así, por ejemplo, si en la fase basal tenemos para el ítem “respiración irregular” una OR = 5,92 podemos concluir que los neonatos que han sido explorados tienen 5,92 veces más posibilidades (riesgo) de tener una respiración irregular en la fase basal que los que no lo han sido.
Resultados
Tal como se refleja en la Tabla 1, Tabla 2 y Tabla 3 correspondientes al momento basal, cambio de pañal y fase de recuperación respectivamente, se observa que, en primer lugar, de los 83 ítems que integran la POS, en 21 no se registró ninguna observación, por lo que retuvimos únicamente aquellos ítems en los que se hubieran obtenido respuestas, quedando finalmente en 62 ítems u observaciones. Dado que lo que interesaba en este estudio era detectar las posibles repercusiones de la exploración oftalmológica en la organización neuroconductual del neonato, en el análisis de los datos únicamente se tuvieron en cuenta las reacciones o signos de estrés. Éstos aparecen destacados en las tablas. En el análisis de las frecuencias obtenidas por ambos grupos (Tablas 1 a 3), se observa que en la primera fase (basal) los neonatos del grupo estudio obtuvieron unas diferencias significativamente superiores a los del grupo control en 6 signos de estrés, mientras que los del grupo control superaron a los del grupo estudio únicamente en uno. En la fase intermedia (cambio de pañal) esta relación fue de 7 signos de estrés observados en el grupo estudio, y 3 en el grupo control.En la fase de recuperación, fueron 9 los signos de estrés observados en el grupo estudio contra únicamente 2 en el grupo control.
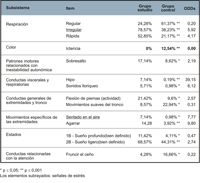
Tabla 1. Frecuencias y porcentajes de cada ítem para los dos grupos y la significación de la prueba de comparación de proporciones en el momento basal.
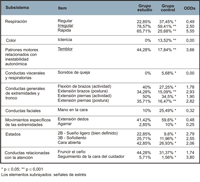
Tabla 2. Frecuencias y porcentajes de cada elemento de los dos grupos y la importancia de la prueba comparativa de proporciones para el período de cambio de pañales.
Tabla 3. Frecuencias y porcentajes de cada elemento de los dos grupos y la importancia de la prueba comparativa de proporciones para el período de recuperación.
Discusión
Los resultados obtenidos aportan datos sobre los efectos negativos en la esfera neuroconductual del neonato prematuro que pueden atribuirse globalmente a la exploración oftalmológica. Los signos de estrés observados en este grupo pertenecen básicamente al sistema autonómico (respiración irregular, sobresaltos, hipo, temblores). Estos signos negativos o de estrés se incrementaron en el transcurso del período de la observación. Teniendo en cuenta que estos signos de estrés fueron significativamente más frecuentes en el grupo estudio que en el grupo control, es plausible suponer que las maniobras implicadas en la exploración oftalmológica son las responsables de esta desestabilización del neonato, puesto que, como se ha dicho, la mayoría de las respuestas pertenecen a la inestabilidad del sistema nervioso autónomo. Por otro lado, cabe recordar que ambos grupos de neonatos eran equiparables, tanto por su edad gestacional como por sus características fisiológicas.No obstante, es difícil dilucidar en este estudio si los efectos observados en la organización neuroconductual del neonato se deben a la maniobra en sí (exploración oftalmológica) o a los efectos colaterales derivados de la potencial absorción sistémica del fármaco. Para ello debería repetirse el experimento utilizando un placebo en lugar de los fármacos habituales y comparar ambos grupos, pero al no ser éticamente aceptable no se plantea su realización.
La aplicación de las medidas descritas en la literatura como, el uso de anestésicos tópicos1,19, ocluir el punto lagrimal para evitar la absorción sistémica en la mucosa nasal10,21,28, disminuir el tamaño de la gota instilada (aprovechando el hecho de que el neonato requiere menores dosis para lograr un mismo efecto farmacológico)29-32, el uso de sacarosa para paliar el dolor y estrés a que se ve sometido el neonato1,25,26, el uso de la anidación como medida de reducción del estrés18, etc. se han mostrado útiles para paliar diversos efectos no deseados fruto de la maniobra exploratoria. Por lo tanto son medidas a considerar para reducir las potenciales causas responsables de los cambios neuroconductuales observados en nuestros neonatos prematuros.
A raíz de este estudio y con el fin de minimizar el estrés que pueda provocar en el neonato la exploración oftalmológica, en nuestra unidad hemos instaurado un protocolo que se aplica tras la realización de esta maniobra de exploración a todos los neonatos. Durante al menos 18 horas, se monitoriza, en el neonato prematuro explorado, la frecuencia cardiaca, la frecuencia respiratoria y la saturación de oxígeno. Se colocan los cubre-incubadoras y se instaura un período de mínima manipulación sobre dichos neonatos. La alimentación se modifica durante ese periodo y se administra por gravedad en lugar de oral, en caso de que el neonato lo requiera.
Agradecimientos
Agradecemos la colaboración de Carlos Navarro por su soporte técnico, así como al grupo de enfermeras formado por Arantxa Muñoz, Joana Archs, Ana Casado, por su ayuda en la recopilación de datos.Este trabajo ha sido realizado con la ayuda recibida del Ministerio Gobierno español de Educación y Ciencia (Proyecto SEJ2007-64856).
Bibliografía
- Coe K. Nursing update on retinopathy of prematurity. JOGNN. 2007;36:288-92.
- Herrero Pérez S, Salvia Roges MD, Rodríguez Miguélez M, Figueras Aloy J, Carbonell Estrany X. Prevención de efectos adversos relacionados con el examen oftalmológico en prematuros. An Pediatr. 2004;60:193.
- Rengstorff RH, Doughty CB. Mydriaric and cycloplegic drugs: a review of ocular and systemic complications. Am J Optom Physiol Opt. 1982;59:162-77.
- Lim Z, Tehrani NN, Levin AV. Retinal haemorraghes in a preterm infant following screening examination for retinopathy of prematurity. Br J Ophthalmol. 2006;90:799-800.
- Rosales T, Isenberg S, Leake R, Everett S. Systemic effects of mydriatics in low weight infants. J Pediatr Ophthalmol Strabismus. 1981;18:42-4.
- Lees BJ, Cabal LA. Increased blood pressure following pupillary dilation with 2.5% phenylephrine hydrochloride in preterm infants. Pediatrics. 1981;68:231-4.
- Merritt JC, Kravbill EN. Effect of mydiatrics on blood pressure in premature infants. J Pediatr Ophthalmol Strabismus. 1981;18:42-6.
- Sindel BD, Baker MD, Maisels MJ, Weinstein J. A comparison of the pupillary and cardiovascular effects of various mydriatic agents in preterm infants. J Pediatr Ophthalmol Strabismus. 1986;23:273-6.
- Ogut MS, Bozkurt N, Ozek E, Birgen H, Kazokoglu H, Ogut M. Effects and side effects of mydriatic eyedrops in neonates. Eur J Ophthalmol. 1996;6:192-6.
- Kumar Nair A, Govind Pai M, da Costa DE, Al Khusaiby SM. Necrotizing Enterocolitis following ophthalmological examination in preterm neonates. Indian Pediatrics. 2000;37:417-21.
- Isenberg SJ, Abrams C, Hyman PE. Effects of cyclopentolate eyedrops on gastric secretory function in pre-term infants. Ophthalmology. 1985;92:698-700.
- Bonthala S, Sparks JW, Musgrove KH, Berseth CL. Mydiatrics slow gastric emptying in preterm infants. J Pediatr. 2000;137:327-30.
- Sarici SU, Yurdakok M, Unal S. Acute gastric dilatation complicating the use of mydriatics in a preterm newborn. Pediatr Radiol. 2001;31:581-3.
- Lim DL, Batilando M, Rajadurai VS. Transient paralytic ileus following the use of cyclopentolate-phenylephrine eye drops during screening for retinopathy of prematurity. J Paediatr Child Health. 2003;39:318-20.
- Shinomiya K, Kajima M, Tajika H, Shiota H, Nakagawa R, Saijyou T. Renal failure caused by eyedrops containing phenylephrine in a case of retinopathy of prematurity. J Med Invest. 2003;50:203-6.
- Aguirre Rodriguez FJ, Bonillo Perales A, Díez-Delgado Rubio J, González-Ripoll Garzón M, Arcos Martínez J, López Muñoz J. Paro cardiorrespiratorio relacionado con examen oftalmológico en prematuros. An Pediatr. 2003;58:504.
- Grabska J, Walden P, Lerer T, Kelly C, Hussain N, Donovan T, Herson V. Can oral sucrose reduce the pain and distress associated with screening for retinopathy of prematurity? J Perinatol. 2005;25:33-5.
- Gal P, Kissling GE, Young WO, Dunaway KK, Marsh VA, Jones SM, Shockley DH, Weaver NL, Carlos RQ, Ransom JL. Efficacy of sucrose to reduce pain in premature infants during eye examinations for retinopathy of prematurity. Ann Pharmacother. 2005;39:1029-33.
- Belda S, Pallás CR, De la Cruz J, Tejada P. Screening for retinopathy of prematurity: is it painful? Biol Neonate. 2004;86:195-200.
- Slevin M, Murphy JF, Daly L, O’Keefe M. Retinopathy of prematurity screening, stress related responses, the role of nesting. Br J Ophthalmol. 1997;81:762-4.
- Als H. Newborn Individualized Developmental Care and Assessment Program (NIDCAP). Boston: Children’s Medical Center Corporation. 1997.
- Ferber SG, Makhoul IR. Neurobehavioural assessment of skin-to-skin effects on reaction to pain in preterm infants: a randomized, controlled within-subject trial. Acta Paediatr. 2008;97:171-6.
- Laws DE, Morton C, Weindling M, Clark D. Systemic effects of screening for retinopathy of prematurity. British Journal of Ophthalmology. 1996;80:425-8.
- Holsti L, Grunau R, Oberlander TF, Whitfield MF. Prior pain induces heightened motor responses during clustered care in preterm infants in the NICU. Early Hum Dev. 2005;81:293-302.
- Pressler JL, Hepworth JT. The effect of gender and race on very preterm neonates’ behavior. Clin Nurs Res. 2002;11:89-102.
- Marsh VA, Young WO, Dunaway KK, Kissling GE, Carlos RQ, Jones SM, Shockley DH, Weaver NL, Ransom JL, Gal P. Efficacy of topical anesthetics to reduce pain in premature infants during eye examinations for retinopathy of prematuruty. Ann Pharmacother. 2005;39:829-33.
- Kleberg A, Warren I, Norman E, Mörelius E, Berg AC, Mat-Ali E, Holm K, Fielder A, Nelson N, Hellström-Westas L. Lower stress responses after Newborn Individualized Developmental Care and Assessment Program Care during eye screening examinations for retinopathy of prematurity: a randomized study. Pediatrics. 2008;121:e1267-78.
- Figueras J, Rodriguez JM, Salvia MD, Botet F. Concerning the article by S. Belda, et al. Screening for retinopathy of Prematurity: is it painful? Biol Neonate. 2006;89:197.
- Belda S, Pallás CR, De la Cruz J, Tejada P. Reply. Biol Neonate. 2006;89:198.
- Saunders RA, Miller KW, Hunt HH. Topical anesthesia during infant eye examinations: does it reduce stress? Ann Ophthalmol. 1993;25:436-9.
- Elibol O, Alcelik T, Yuksel N, Caglar Y. The influence of drop size of cyclopentolate, phenylephrine and tropicamide on pupil dilatation and systemic side effects in infants. Acta Ophthalmol Scand. 1997;75:178-80.
- Wheatcroft S, Sharma A, McAllister J. Reduction in mydriatic drop size in premature infants. Br J Ophthalmol. 1993;77:364-5.